理学療法士は患者に合わせた歩行をデザインすることが業である。そうであれば、歩行の「しくみ」を知ることがデザインの質を高めることにつながる。
ヒトが2足歩行を獲得してから約400万年が経つ。石器時代では、獲物を捕るため動物の動きに集中したり、敵の攻撃を回避するために周囲を気にしながら歩く必要があった。その際、歩行に意識を向けているようでは獲物を逃し、敵の攻撃から身を守ることは困難だろう。ヒトが生き延びるためには、歩行を自動化させ、環境に意識を向けることが進化の過程で淘汰されないための手段であったのだ。
進化の過程で得た歩行の自動化は、現在の生活でも必要な機能となっている。私たちはスマホを見ながら、あるいは友達とおしゃべりしたり、綺麗な桜に目を奪われながら歩くことができる。日常生活において歩くことを意識することはほとんどない。言い換えると、歩行を意識していると日常生活は成り立たないのである。歩行の自動化は、生活の質を維持するために必要な機能なのだ。

では、この自動化された歩行は、何によって制御されるのだろうか。その制御機構がCPG(central pattern generator)なのである。
Table of contents
◆ 偶然の中で発見されたヒトのCPG
1911年、Graham-Brownらは、脊髄ネコ(脊髄を切断したネコ)の実験により、脳からの入力や感覚のフィードバックなしにリズミカルな下肢の運動パターンを生成する機能が脊髄にあることを発見した。そして1985年、Grillnerらは、これらの神経回路が腰仙部にあり、ステッピング様の運動パターンを作り出すことが可能であることを示唆し、これを「CPG」と呼んだ。
1990年代に入ると、ネコや犬、ウサギなどの哺乳類だけでなく、サルにもCPGが存在することが示された。これにより、ヒトにもCPGが存在するだろうという推測が研究者の間で認知されていった。しかし、ヒトはネコなどのように除脳や脊髄切断を実験的に行えない。そのため、ヒトのCPGの存在はなかなか推測の域を超えなかった。
1998年、Dimitrijevicらは、脊髄損傷患者の下肢の痙性抑制を抑制する目的で、腰髄を電気刺激する実験を行った。その際、刺激の周波数を調整していると、突然、麻痺した下肢が交互に動き出すことを発見したのである。
そこでDimitrijevicらは、6名の脊髄損傷(C5-Th8)患者を対象に、針電極を用いて、腰髄レベルで刺激部位と周波数を変えながら電気刺激を行い、下肢筋の筋電図、膝の可動域を測定した。
その結果、L2レベルを25-50Hzの周波数で刺激すると、下肢のステップ様運動がみられるとともに、筋電図が記録された。筋電図は、大腿四頭筋、ハムストリングス、前脛骨筋、下腿三頭筋と膝、足関節の伸筋、屈筋を対象に導出しており、電気刺激によって伸筋、屈筋が交互に収縮する様子をとらえた。また、それに合わせて膝の屈曲が行われており、ステッピング様の運動が認められたのだ。この研究により、初めてヒトのCPGの存在が示されたのである(Fig 1)。

(Fig 1:Dimitrijevic, 1998より改変)
◆ CPGモデルから考える感覚入力の重要性
動物、ヒトのCPG研究とともに、神経生理学によるCPG制御モデルの検討が並行して行われた。CPG制御モデルは諸説あるが、基礎となっているのは「half-centerモデル」である。CPGでは、屈筋・伸筋の興奮性ニューロンが並列になってコントロールしていることからhalf-centerと呼ばれている。それでは、このhalf-centerモデルを用いて、Dimitrijevicらの研究結果をシュミレートしてみよう(Fig 2)。
 (Fig 2)
(Fig 2)
①硬膜外から電気刺激がCPGに届くと、ニューロン1は、伸筋の運動神経を興奮させ、伸筋を収縮させる。
②同時にニューロン1は、抑制性の介在ニューロン2を興奮させ、ニューロン3の興奮を抑制し、屈筋は弛緩する。
③介在ニューロン2の活動が減弱(fatigue)すると、ニューロン3の抑制が解除され、屈筋の運動神経を興奮させ屈筋を収縮させる。
④ニューロン3が活性化すると、抑制性の介在ニューロン4を通じて、ニューロン1の活動を抑制し、伸筋は弛緩する。
このように、硬膜外刺激がCPGにある2つの興奮性ニューロンを興奮させ、抑制性の介在ニューロンを介して伸筋、屈筋が交互に収縮、弛緩し、膝関節のリズミカルな屈伸運動が出力されるのである。
Dimitrijevicらにより、腰髄膨隆部を電気刺激すると下肢の交互運動が出現することが示された。さらに、Jilgeらは、刺激周波数の違いにより伸筋、屈筋の固有の収縮が認められることを示した。完全対麻痺患者5名の腰髄膨隆部近辺を5-15Hzで刺激すると下肢の伸筋群の収縮が誘発され、下肢全体を突っ張るような運動が出現したのに対して、それより高い周波数25-50Hzで刺激するとステッピングに似た屈曲運動が出現されたという(Fig 3)。
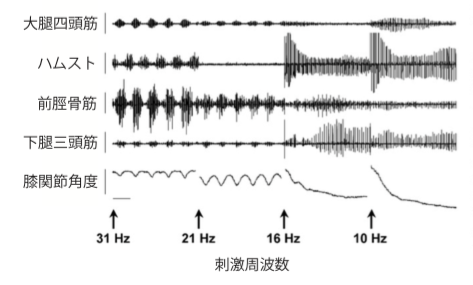
(FIg 3:Jilge, 2004より改変)
この結果から、CPGは入力される刺激の周波数が低い場合は伸筋が収縮し、高い場合は屈筋が収縮するという刺激入力依存性を有していることが示唆された。
また、Gurfinkelらは、健常者を対象に、下肢の筋あるいは腱への振動刺激でエアーステッピングが誘発できることを示した。この結果は、求心性の感覚入力がCPGの発生に寄与していることを示唆している(Fig 4)。

(Fig 4:Gurfinkel, 1998)
これらの報告から、CPGは末梢からの感覚入力と相互作用によって、伸筋、屈筋の異なる運動を生成すると解釈されている。CPGの刺激入力依存性により、脳からの下行性入力に加え、末梢からの感覚入力が合わさることによって運動パターンの生成が変化することが推測される。つまり、ヒトの歩行は自動化されているが、その運動生成には末梢からの感覚入力が大きな役割を担っているのである。
それでは、先ほど示したCPGのhalf-centerモデルに感覚入力を加えてシュミレートしてみよう。感覚入力は、伸筋側のみを示している(屈筋側は省略)。
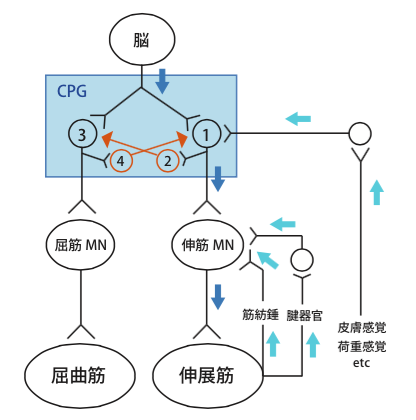
①脳からの下行性入力がCPGのニューロン1を興奮させ、その興奮は伸筋の運動ニューロンにつ伝わり、伸筋が収縮する。
②伸筋が収縮すると、筋紡錘や腱、皮膚や圧受容器からのフィードバックがCPG、伸筋の運動ニューロンに入力され、CPGの促通や抑制が行われる。
このように感覚入力がCPGや運動ニューロンにフィードバックされることでリズミカルな歩行様運動は洗練され、より安定性の高い運動になるのである。
それでは、どのような感覚入力がCPGに大きく寄与するのか?次回、考察してみよう。
◆ 知っておきたい参考記事
歩行のしくみ①:CPGについて考えよう
歩行のしくみ②:歩行適応について考える
歩行のしくみ③:歩行適応の神経メカニズム
歩行のしくみ④:歩行を早く適応させる2つの方法
歩行のしくみ⑤:歩行を早く適応させる2つの方法・その2
歩行のしくみ⑥:歩行の起源
歩行のしくみ⑦:歩き方をデザインする基準
歩行のしくみ⑧:歩行適応における踵接地の役割
歩行のしくみ⑨:加齢により歩行の適応能力は変化する?①
歩行のしくみ⑩:加齢により歩行の適応能力は変化する?②
歩行のしくみ⑪:歩行速度で余命を予測しよう
歩行のしくみ⑫:歩行速度で転倒リスクを予測しよう
歩行のしくみ⑬:脳卒中後の歩行速度とQOL
歩行のしくみ⑭:生体力学が教える速く歩くためのポイント
歩行のしくみ⑮:生体力学が教える速く歩くためのポイント②
歩行のしくみ⑯:脳卒中の発症部位と歩行速度
歩行のしくみ⑰:ヒトの皮質網様体路と歩行制御
Reference
Graham-Brown T, et al. (1911) The intrinsic factors in the act of progression in the mammal. Proc R Sopc Lond B Biol Sci, 84:308–319.
Grillner S, et al. (1985) Neurobiological bases of rhythmic motor acts in vertebrates. Science, 228(4696):143–149.
Dimitrijevic, M. R, et al (1998). Evidence for a spinal central pattern generator in humans. Annals of the New York Academy of Sciences, 860, 360–376.
Jilge, B., et al (2004). Frequency-dependent selection of alternative spinal pathways with common periodic sensory input. Biological Cybernetics, 91, 359–376.
GurWnkel, V. S., et al (1998). Locomotor-like movements evoked by leg muscle vibration in humans. The European Journal of Neuroscience, 10, 1608–1612.
「説明がわからない」「これが知りたい」などのご意見はTwitterまでご気軽にご連絡ください。