8月14日、外傷性脳損傷に対するヒトの幹細胞を脳に直接注入して機能回復を試みる治験を東大病院が始めることが報道されました。
最近では、再生医療が脳卒中や脊髄損傷治療のパラダイムシフトを起こし、リハビリテーションの役割も大きく変わるのでは?という話題もよく聞きます。
そこで、今回は、2016年6月に雑誌Strokeに掲載された脳卒中の再生医療に関する最新の論文をご紹介します。
リハビリテーションに関わる医療者として、再生医療の「今」を知っておくことは、今後の医療の移り変わりを予測するためにも有用でしょう。
現在の脳卒中治療は、主に急性期に行われる血栓溶解療法(t-PA)や動脈内血栓除去術などに限らています。亜急性期から慢性期ではリハビリテーションが後療法として実施され、その効果も6ヶ月でプラトーに達するとされています。
これは、脳の神経成長促進因子の働きが、急性期にピークを迎え、発症後1ヶ月を経過すると逆に神経成長抑制因子の働きが高まることが要因として考えられています。

そのため、慢性期の脳卒中治療が、医師やリハビリ従事者の大きな研究テーマになっているのです。
脳卒中の再生医療では、使用する細胞や細胞を投与する手段が数多くあり、その一つ一つの効果が検証されてきました。
2013年、幹細胞を用いた研究グループであるPISCES(Pilot Investigation of Stem Cells in Stroke)の報告(Phase Ⅰ)によって、細胞はヒトの骨髄間葉系幹細胞が、投与方法は脳内投与が最も効果的であることが示されました(Kalladka D, 2013)。さらに、2014年に報告された脳卒中の再生医療のメタアナリシスにおいても、同様の結果が認められたのです(Vu Q, 2014)。
これらの研究結果から、PISCES PhaseⅡでは、ヒトの骨髄間葉系幹細胞の脳内投与による安全性と機能回復の効果について、2年間の臨床試験を開始しました。
2016年6月、スタンフォード大学のSteinbergらは、PISCES PhaseⅡの暫定結果として、慢性期脳卒中患者を対象に、ヒトの骨髄間葉系幹細胞の脳内投与後、12ヶ月間の安全性と機能改善のデータを報告しています。
対象は、発症から平均22ヶ月が経過した軽度〜中等度の慢性期脳卒中患者18名(平均年令61歳)です。
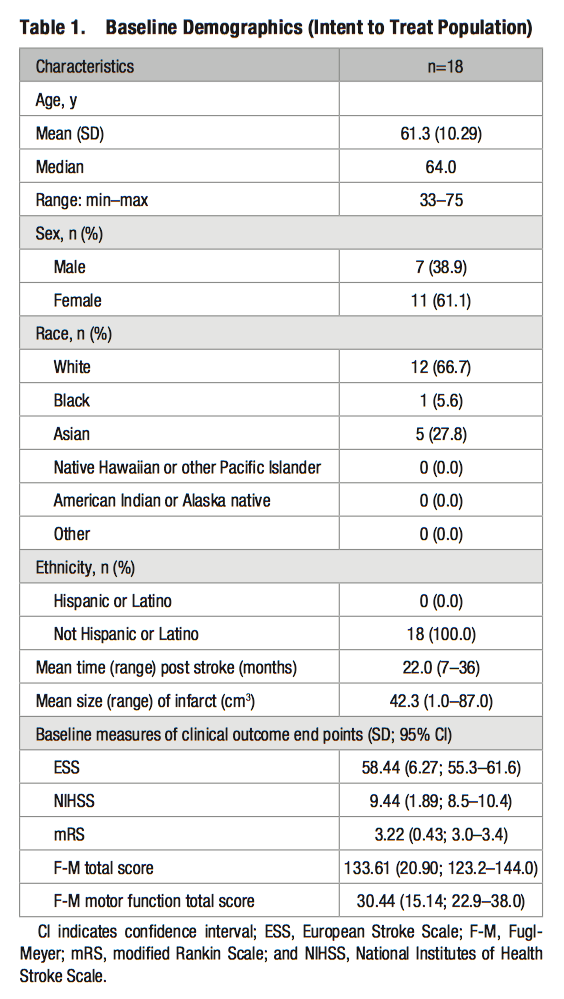
Fig.1:Steinberg GK, 2016より引用
尚、臨床試験の間、対象者はリハビリテーションを全く行っていません。
機能改善のアウトカムは、ESS(European Stroke Scale)、NIHSS(National Institutes of Health Stroke Scale)、Fugl-Meyer total score、Fugl-Meyer motor function total score、mRS(modified Rankin Scale)の5つです。
*ESS、NIHSSはクリックするとPDFページに移動します。
また、MRI所見も同時に調査しました。
臨床試験開始から12ヶ月の時点で、外科術後の合併症のために脱落した2名を除く16名の調査結果では、幹細胞の脳内投与による合併症は認められませんでした。
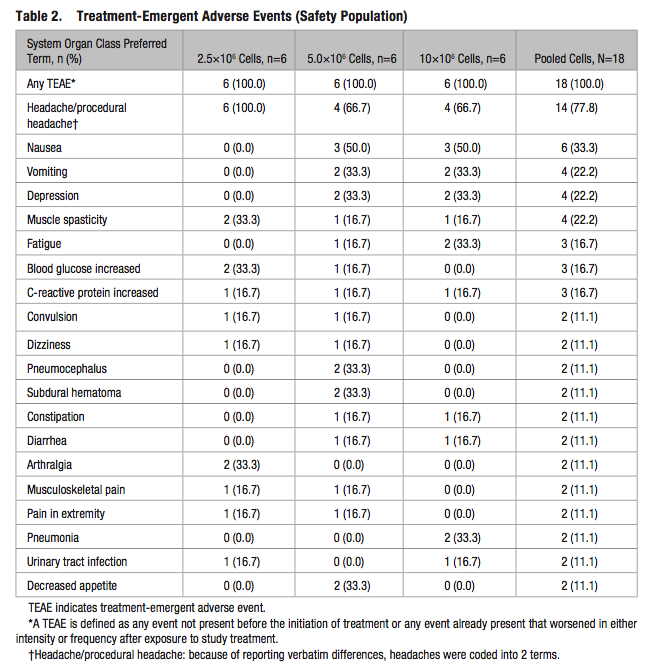
Fig.2:Steinberg GK, 2016より引用
12ヶ月後の機能回復では、ESS、NIHSS、Fugl-Meyerのtotal score、Fugl-Meyerのmotor function total scoreで有意な改善が認められました。mRSには改善が認められませんでした。

Fig.3:Steinberg GK, 2016より引用
MRI所見では、投与後1週間で同側の皮質に改善を示す信号変化が認められました。
これらの結果から、ヒトの骨髄間葉系幹細胞の脳内投与は、投与後12ヶ月の時点で、安全性が示され、機能回復に大きく寄与することが示唆されたのです。
特に改善が認められたFugl-Meyerの運動機能は、慢性脳卒中患者の機能改善に対して信頼性、妥当性のある評価方法とされています(Sullivan KJ, 2011)。また、Fugl-Meyerの運動機能スコアにおける10ポイント以上の改善は、慢性脳卒中患者の明らかに意味のある変化として受け入れられています(Page SJ, 2009)。
今回の結果では、12ヶ月間、リハビリテーションを行っていないにも関わらず、Fugl-Meyerの運動機能スコアが平均11.4ポイントも改善しており、幹細胞の脳内投与が慢性期の脳卒中患者の運動機能改善に有効であることを示しているとSteinbergらは述べています。
また、有意な改善が認められなかったmRSは、一般的に急性期で用いられるアウトカムであるため、慢性期を対象にした今回の調査では変化が見られなかったのだろうと推測しています。
今回のヒトの骨髄間葉系幹細胞の脳内投与における12ヶ月後のポジティブな結果をもとに、PISCESでは、今後、投与から2年後の調査結果であるPISCES PhaseⅡbを報告し、さらに大規模なPhaseⅢへ臨床試験を進めていくことを予定しているとのことです。
紹介したPISCES PhaseⅡの報告は、2011年から2013年の2年間で行われた調査をもとにしたものなので、PhaseⅡbの報告も近いうちに行われるでしょう。そして、現在では、すでにPhaseⅢへ調査は移行している可能性もあります。引き続き、PISCESの報告を本ブログでは追っていきます。
脳卒中の再生医療が臨床応用されれば、急性期ではt-PAや血栓除去術、血腫除去術を行い、慢性期では再生医療を行うという期間に応じた医学的治療が期待できるでしょう。
このような脳卒中治療のパラダイムシフトの中でリハビリテーションの役割も大きく変わるかもしれません。再生医療とリハビリテーションについて、再生医療が機能回復を引き起こすメカニズムやリハビリがどのように改善に寄与できるかなど、今後も最新の知見をご紹介していきたいと思います。
Reference
Kalladka D, et al. Pilot Investigation of Stem Cells in Stroke (PISCES). A phase 1 trial of CTX0E03 human neural stem cells. Cerebrovasc Dis. 2013;35(suppl 3):551.
Vu Q, et al. Meta-analysis of preclinical studies of mesenchymal stromal cells for ischemic stroke. Neurology. 2014 Apr 8;82(14):1277-86.
Steinberg GK, et al. Clinical Outcomes of Transplanted Modified Bone Marrow-Derived Mesenchymal Stem Cells in Stroke: A Phase 1/2a Study. Stroke. 2016 Jul;47(7):1817-24.
Sullivan KJ, et al. Fugl-Meyer assessment of sensorimotor function after stroke: standardized training procedure for clinical practice and clinical trials. Stroke. 2011 Feb;42(2):427-32.
Page SJ, et al. Modified constraint-induced therapy combined with mental practice: thinking through better motor outcomes. Stroke. 2009 Feb;40(2):551-4.